
TOP Labo Members Research Publications Presentations Link
Photo
研究テーマ
1. 細胞内で産生される機能性代謝産物の機能解明とその応用
2. β-1,3-1,6-グルカンナノ粒子を用いた難水溶性食品、化粧品、医薬品成分の可溶化とその応用
3. 主鎖へ機能性分子をコンジュゲートした機能性核酸の開発
4. β-1,3-グルカン多糖の部位特異的化学修飾法の開発と遺伝子キャリアーへの改変
[1. 細胞内で産生される機能性代謝産物の機能解明とその応用]
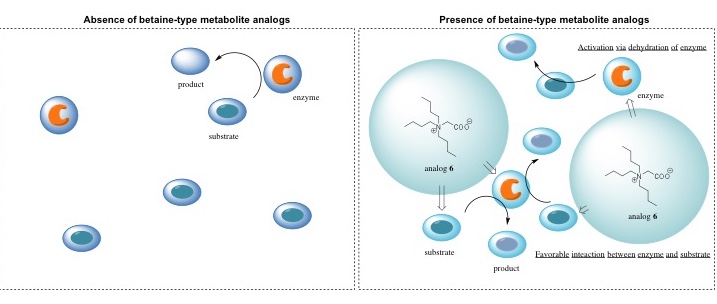
■ ベタイン型代謝産物アナログの添加によるα-グルコシダーゼによる加水分解反応の速やかな活性化/安定化
Quick Activation/Stabilization of a alpha-Glucosidase-Catalyzed Hydrolysis Reaction by Addition of a Betaine-Type Metabolite Analogue
Shiro Sehata, Yuichi Nakagawa, Ryutaro Genjima, Kazuya Koumoto
Chem. Lett., 45, 1174-1176 (2016)
これまでに報告からベタイン型の代謝産物アナログを反応溶液に混合すると、酵素反応が促進されることが報告されてきた。酵素活性化剤では、酵素と活性化剤を混合後、相互作用するように予備恒温等を行うものが多いが、このアナログも同じような活性化を示すのか、に興味が持たれた。本研究では恒温され、基質と反応中の酵素溶液にアナログを事後添加し、その活性化挙動を調べた。その結果、アナログは添加されると速やかに酵素を活性化した。しかし、時間が経過して溶液中の酵素が失活している溶液中では活性化が起こりにくかった。これは本アナログが変性、失活した酵素をリフォールディンングすることなく、活性を保持した酵素のみを活性化することを示唆するものであった。また、溶液中にアナログを添加すると、酵素の経時的な安定性が上昇すること、特に希薄溶液中での酵素の安定化に効果を発揮することも明らかとなった。
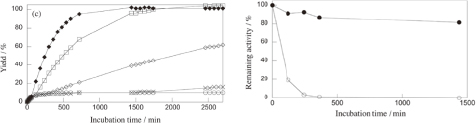
■ 酵素反応の促進におけるベタイン型代謝産物アナログのアニオン性官能基の重要性
Significance of anionic functional group in betaine-type metabolite analogs on the facilitation of enzyme reactions
Yuichi Nakagawa, Kotomi Takagi, Ryutaro Genjima, Kazuya Koumoto
Bioprocess Biosys. Eng., 38, 1811-1817 (2015)
これまでに報告からベタイン構造を有する代謝産物アナログが酵素反応の促進に効果を示すことが報告されてきた。アナログライブラリーを用いた研究から、この活性化はアンモニウム基に極性原子団を含まないアルキル鎖を入れることが効果的であるとされてきたが、アニオン性官能基の効果については議論がされてこなかった。そこで本論文では、アニオン性官能基の重要性を評価するために新たにスルホベタインのライブラリーを合成し、酵素活性化挙動をカルボキシベタインと比較した。その結果、最大活性化濃度、最大活性比ともに違いがなく、アニオン性官能基は酵素活性化には影響を及ぼさないことが明らかとなった。また、ベタイン構造であることの特徴を考察するために、分子間の対イオンであるテトラアルキルアンモニウム塩でも同じ比較を行ったところ、アルキル鎖の伸長に伴う最大活性化濃度の低下はベタインよりも効果が弱まり、最大活性比はベタイン誘導体の半分に低下した。今回の結果は、以前に報告したTetrahedron, 70,5895-5903 (2014)の結果を合わせ、酵素活性化に寄与する最適なベタイン誘導体の分子設計に関する知見を与えるものと考えられる。
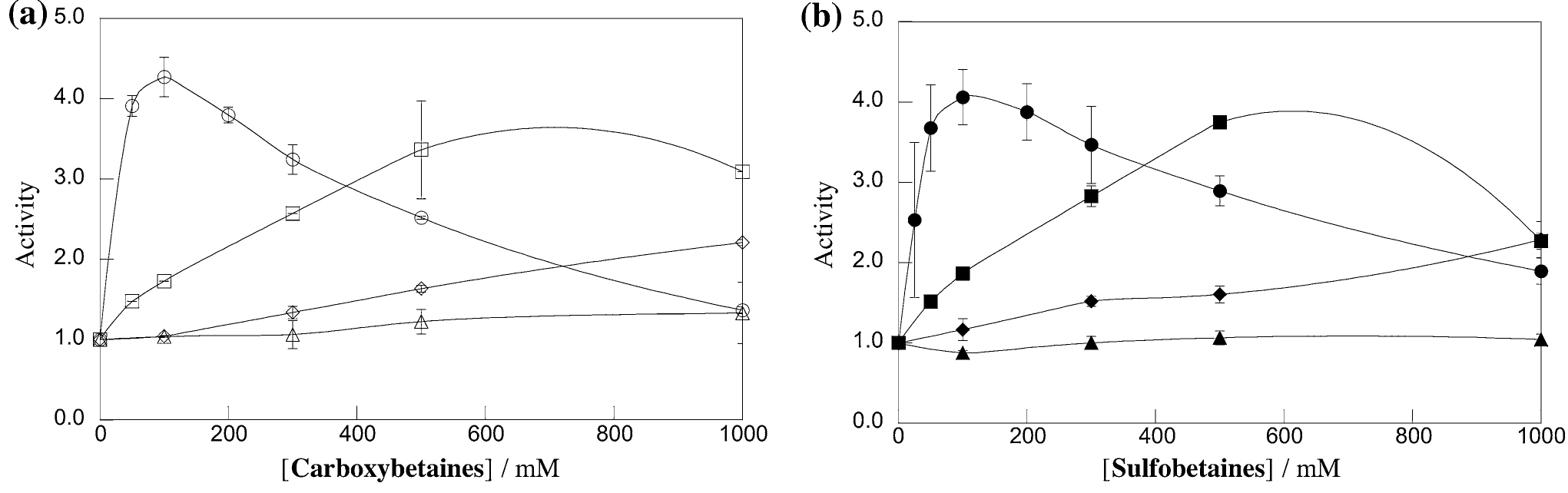
■ ベタイン型代謝産物アナログの存在下での西洋ワサビ由来ペルオキシダーゼによる酸化触媒反応の発色感度の向上
Enhanced Chromogenic Sensitivity of Horseradish Peroxidase-catalyzed Oxidative Reactions in the Presence of Betaine-type Metabolite Analogs
Kotomi Takagi, Yasuhiro Kashima, Satoshi Fujii, Kazuya Koumoto
Bull Chem. Soc. Jpn., 88, 1074-1082 (2015)
これまでに報告してきたベタイン型代謝産物アナログを用い、標識酵素として臨床検査に利用される西洋ワサビ由来ペルオキシダーゼ(HRP)の活性化について評価した。HRPには多種多様な発色基質があるが、ABTS、Trinder試薬、TMB、ASA、DAB、AECといった構造が異なる基質に対してアナログは共通して濃度依存的な活性化効果を示した。速度論パラメーター解析の結果から、活性化はVmax(kcat)に依存して生じることが明らかとなった。またここで明らかとなったのは、他の酵素ではアナログの添加によってKmが低下したが、HRPではその値は上昇し、アナログの添加により基質の結合性が低下することが明らかとなった。しかし、この親和性の低下はHRPにとって好適に働き、HRPはアナログを添加すると基質に加え、生成物の結合性も弱めていた。実際、アナログを添加すると、生成物阻害の抑制によって発色量が増加した。これはヘム周辺のペプチド鎖の揺らぎによることがCDスペクトル、ESRスペクトルから確かめられた。また、このような生成物阻害による発色感度の上昇は、ウェスタンブロッティングにおいても検出下限を低下させ、効果を発揮することが実証された。
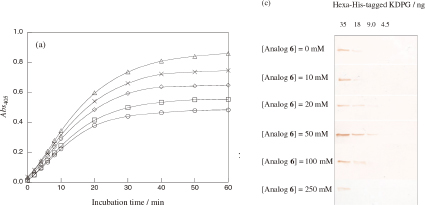
■ 酵素の凍結変性に及ぼすベタイン型代謝産物アナログの凍結保護効果
Cryoprotective ability of betaine-type metabolite analogs against freeze denaturation of enzymes
Yuichi Nakagawa, Masahiro Sota, Kazuya Koumoto
Biotechnol. Lett., 37, 1607-1613 (2015)
我々の研究室では、細胞内に高濃度で蓄積する代謝産物の化学構造とそれがもたらす細胞機能との相関を明らかにするために、グリシンベタインを基体としたアナログライブラリーを合成し、酵素活性に及ぼす構造効果について検討してきた。このような代謝産物には氷点下の極海において、細胞機能を保護するものも存在する。本研究では、凍結によって引き起こされるタンパク質(酵素)の変性に及ぼす代謝産物アナログの添加効果について評価、検討した。その結果、代謝産物アナログを酵素凍結溶液に共存させると、構造依存的、濃度依存的に酵素を凍結変性から保護する効果が発現した。また、その効果は特定の酵素だけに働くわけではなく、αーグルコアシダーゼ、βーグルコシダーゼ、アルカリフォスファターゼ、スルファターゼ、乳酸脱水素酵素、西洋ワサビペルオキシダーゼといった基質や反応機構の異なる種々の酵素群に効果を発揮した。αーグルコシダーゼを用いて凍結・解凍を繰り返した実験では、100回凍結・解凍を繰り返してもその活性は95%以上保持されていることが明らかとなった。
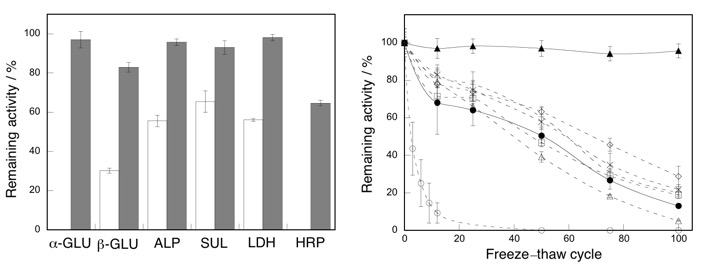
■ ベタイン型代謝産物アナログ存在下におけるαーグルコシダーゼの活性化機構解析
Mechanistic study on the facilitation of enzymatic hydrolysis by α-glucosidase in the presence of betaine-type metabolite analogs
Yuichi Nakagawa, Shiro Sehata, Satoshi Fujii, Hiroaki Yamamoto, Akihiko Tsuda, Kazuya Koumoto
Tetrahedron, 70,5895-5903 (2014)
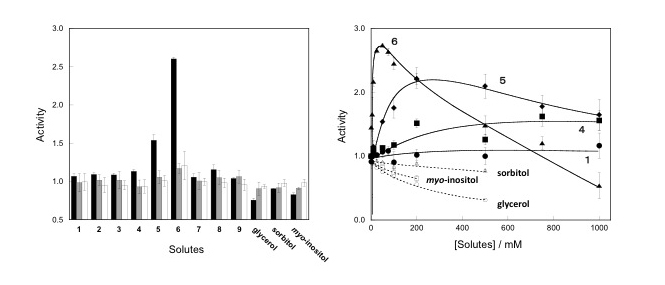
これまでの研究からベタイン構造を有する代謝産物のアナログが構造依存的に酵素を活性化することが明らかとなっている。本研究では、その活性化機構を明らかとするためにライブラリーの拡充とベタイン水溶液の溶液物性解析を行った。ライブラリの拡充に伴う構造相関からは、アンモニウム基にC1〜C7の炭化水素鎖を導入すると、炭素鎖が1つ伸長するごとに酵素活性化に要するアナログの添加濃度が一桁低下することが示され、C7(n-ペンチル基)ではわずか50μMで酵素を活性化させることを可能とした。また、ベタイン水溶液の溶液物性解析から、ベタインは水溶液中でモノマー分散しており、疎で大きな水和層を持つことが明らかとなった。この水和層は密に水和された親水性物質をその水和層から排他し、酵素—基質の相互作用を増強すると推察される。以上のように、ベタイン構造を有する代謝産物アナログによる酵素活性化は疎水性のアルキル鎖表層での特異な水和による間接的な活性化であることが示唆された。
■ 細胞内の対イオン型代謝産物アナログによるα−グルコシダーゼの反応速度、熱安定性、耐塩性、基質選択性の向上
Cellular zwitterionic metabolite analogs simultaneously enhance reaction rate, thermostability, salt tolerance, and substrate specificity of alpha-glucosidase
Bioorg. Med. Chem., 19, 3128-3134(2011)
我々の研究室では、細胞内に高濃度で蓄積する代謝産物の化学構造とそれがもたらす細胞機能との相関を明らかにするために、グリシンベタインを基体として、化学構造に多様性をもたせた対イオン型代謝産物アナログライブラリーを合成してきた。これまでの研究によって、このアナログを溶液中に共存させると、代謝産物の化学構造依存的にDNA二重鎖を不安定させることが明らかとなっている。本研究では、これら代謝産物アナログが酵素活性にいかなる影響を及ぼすかについて、α−グルコシダーゼ、β−グルコシダーゼ、アルカリフォスファターゼのような加水分解酵素を用いて評価、検討した。その結果、アナログの化学構造に依存して酵素の加水分解速度を上昇させることが見出された。α−グルコシダーゼを用いた速度論解析の結果、反応速度の上昇は基質・酵素の結合性の上昇(Km値の低下)と濃度依存的な触媒活性の上昇(Vmax値の上昇)によってもたらされることが明らかとなった。また、代謝産物アナログを反応溶液に添加すると、反応速度だけでなく、酵素の熱安定性、耐塩性、基質選択性も同時に向上することが明らかとなった。
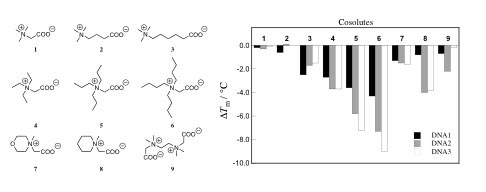
■ 代謝産物の化学構造が二重鎖DNAの安定性に及ぼす影響とポリメラーゼ連鎖反応(PCR)における添加剤としての応用
Structural effect of synthetic zwitterionic cosolutes on the stability of DNA duplexes
Tetrahedron, 64, 168-174(2008)
代謝産物といわれると、ATP生産過程における副産物として細胞外に排出される老廃物と考えてしまいがちである。しかし、細胞は、乾燥、高塩、高温、低温といった危機的環境に直面すると、細胞内に代謝産物を高濃度で産生、蓄積する。また、細胞外環境によってこれらの代謝産物は使い分けられることが知られているが、なぜそれらの代謝産物が使われるのか、その理由は今もわからないことが多い。我々の研究室では、代謝産物の化学構造とそれがもたらす細胞機能との間には相関があるのではないかと仮説を立て、有機合成的手法を用いて代謝産物の化学構造に関連性を持たせたアナログライブラリーを合成し、生体高分子の主要構造の一つであるDNA二重鎖の安定性に対する効果を評価、検討した。その結果、代謝産物の化学構造のわずかな違いによってDNA二重鎖の安定性に大きな差が生ずることを明らかとした。また、DNA二重鎖を不安定化することを利用して、ポリメラーゼ連鎖反応(PCR)における添加剤(融点低下剤)として利用したところ、DNAの増幅を促進することが明らかとなった。
[2. β-1,3-1,6-グルカンナノ粒子を用いた難水溶性食品、化粧品、医薬品成分の可溶化とその応用]
■ 変性β-1,3-1,6-グルカンナノ粒子との複合体形成を利用する難水溶性生理活性物質の中性水溶液中への可溶化
Solubilization of poorly water-soluble bioactive molecules in neutral aqueous media by complexation with renatured β-1,3-1,6-glucan nanoparticles
Biopolymers, 111, e23349(2020)
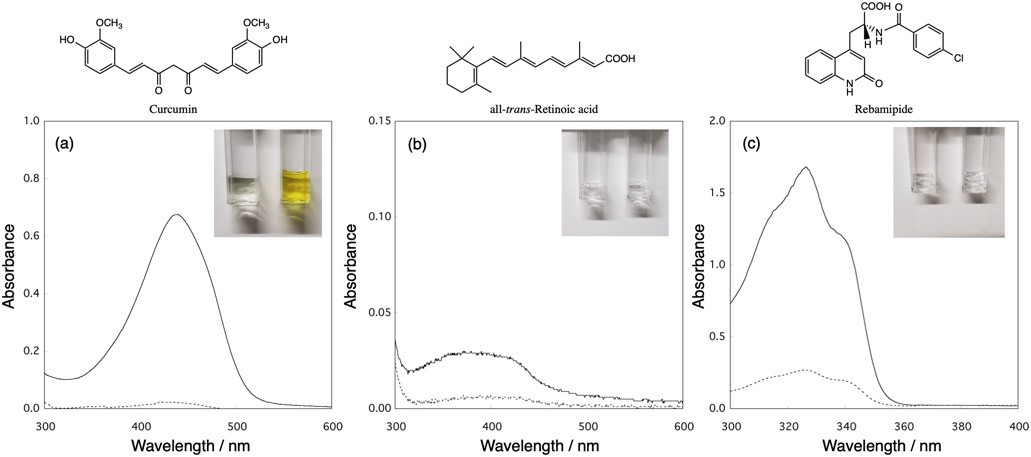
難水溶性の生理活性物質を安定に中性水溶液中に溶解/分散させる技術は機能性食品、医薬品、化粧品の分野で必要とされている。3重螺旋構造を形成するβ-1,3-1,6-グルカンは螺旋構造内部に疎水空間を有する。これまでアルカリやDMSOで1本鎖に融解した後、疎水物質と共存させ、中和や透析によって複合体を形成していたが、この方法ではアルカリで分解したり、DMSOに溶解しない物質には適用できなかった。本論文で我々はアルカリ変性後、再溶解して調製されるrenatured β-1,3-1,6-グルカン(r-glucan)を新しいホストとして注目した。r-glucanは高濃度で調製するとポリマー鎖のネットワーク形成のためにゲル化して塊状物が形成されるが、塊状物ができない中程度の濃度で調製し、遠心分離操作を行うと16 nm程度のナノ粒子が形成されることが明らかとなった。この粒子は遠心分離を繰り返しても沈殿せず、中性水溶液中で難水溶性物質を混合するだけで、食品、医薬品、化粧品関連の構造の異なるゲスト分子と包接複合体を形成する。内部の疎水空孔にゲスト分子はスタッキングされ、J会合体として包接されるため、同一の総グルコース濃度においてシクロデキストリンよりも20%も多く包接が可能で、加えて、1ヶ月に渡ってゲストを徐放する特性を有すことが明らかとなった。アルカリで分解されるような食品、医薬品、化粧品関連の生理活性物質に対する新しい徐放性キャリアとしての用途が期待される。
[3. 主鎖へ機能性分子をコンジュゲートした機能性核酸の開発]
■ ヘアピンDNAのループ部位へアゾベンゼンを導入した光応答性核酸
Reversible stability switching of a hairpin DNA via a photo-responsive linker unit
Chem. Commun., 1915 - 1917(2009)
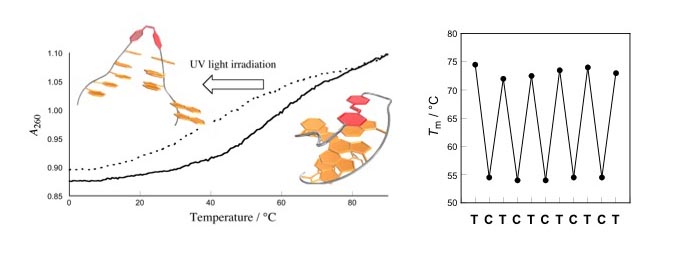
光反応は、高速で、且つ、系内に余分な試薬を添加することのないクリーンな反応として多くの化学システムで利用されている。我々は、このような特性を持つ代表的な分子“アゾベンゼン”をヘアピンDNAに導入し、光によるヘアピンDNAの安定性の制御を試みた。これまでにスチルベン、アゾベンゼンをヘアピンDNAのループ部位に導入した報告は多くあるが、光異性化によってヘアピンDNAの安定性を制御できた報告はない。その原因は、これまでに導入してきた光応答性ユニットの多くでDNAとの連結に必要なリンカーユニットが必要以上に長く柔軟であると考え、ループ長とほぼ等しい4,4’-ビス(ヒドロキシメチル)アゾベンゼンを設計、合成し、DNAのループ部位に導入した。また、リンカー長が長い4,4’ -ビス(ヒドロキシエチル)アゾベンゼンをコントロールとしてリンカー長がヘアピンDNAの安定性に与える影響を検討した。その結果、2つのアゾベンゼンユニットは紫外光、可視光によって同程度の光異性化を受けるが、ヘアピンDNAのループ長と同じ長さの4,4’-ビス(ヒドロキシメチル)アゾベンゼンのみがヘアピンDNAの安定性を光可逆的に制御できることが明らかとなった。このユニットは繰り返しの異性化でも安定性はほとんど変わらず、また、光によって20℃近くの安定性の違いを生み出すことができることから、今後、このユニットを利用した光応答性の核酸医薬等への応用が期待される。
[4. β-1,3-グルカン多糖の部位特異的化学修飾法の開発と遺伝子キャリアーへの改変]
■ 多糖・核酸複合体6 −相補鎖添加に伴う多糖複合体からの核酸の放出ー
Polysaccharide/Polynucleotide Complexes Part 6 -Complementary-Strand-Induced Release of Single-Stranded DNA Bound in the Schizophyllan Complex
Chem. Biodiv., 1, 520 - 529(2004)
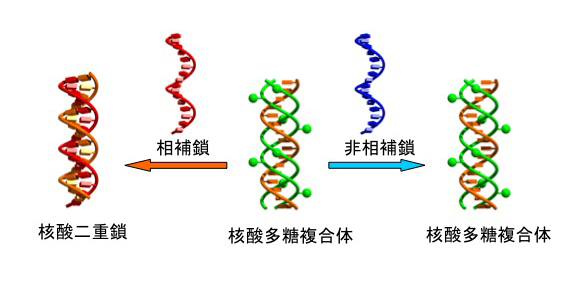
スエヒロダケと呼ばれるキノコが産生するシゾフィラン(β−1,3グルカン)は3重らせん構造を形成している。我々は3重鎖構造を変性させた後、ある種の一本鎖核酸を共存させた状態でランダムコイル構造から3重鎖へシゾフィランを巻き戻させると3本の多糖鎖の1本が核酸に置き換わった多糖・核酸複合体が形成されることを報告している。本論文では、その多糖・核酸複合体に相補鎖および非相補鎖核酸を添加し、多糖核酸複合体の構造変化を分光学的手法で解析を行った結果を報告している。多糖・核酸複合体は生理条件下で非常に安定な高分子複合体を形成しているが、溶液中に相補鎖核酸を添加すると高分子複合体に取り込まれた核酸が放出されることが確認された。これは非相補鎖核酸を添加しても確認されず、相補鎖核酸を添加させたときのみに特異的に起こる現象であることが確認された。この現象はシゾフィランを遺伝子を運搬するキャリアーとして利用したときの有効性を示すものである。
■ 多糖・核酸複合体9 −部位特異的化学修飾法を利用したシゾフィラン側鎖グルコース残基へのカチオン電荷の導入とそれに伴うシゾフィラン-Poly(C)複合体の熱安定化ー
Chemical modification of schizophyllan by introduction of a cationic charge into the side chain which enhances the thermal stability of schizophyllan–poly(C) complexes
Chem. Commun., 1962 - 1963(2001)
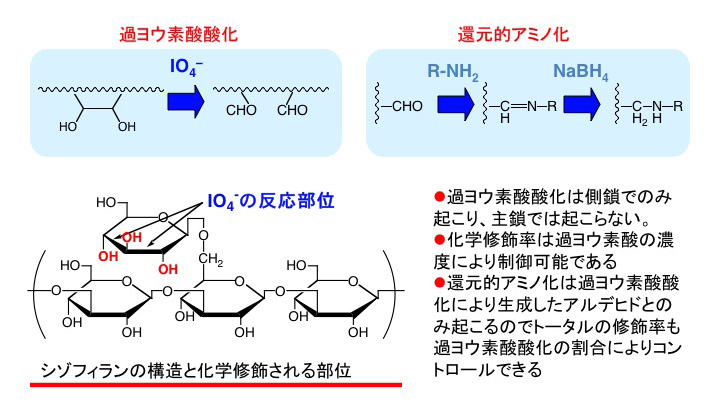
スエヒロダケが産生するシゾフィラン(β−1,3グルカン)は3重らせん構造を形成している。我々は3重鎖構造を変性させた後、ある種の一本鎖核酸を共存させた状態でランダムコイル構造から3重鎖へシゾフィランを巻き戻させると3本の多糖鎖の1本が核酸に置き換わった多糖・核酸複合体が形成されることを報告している。本論文では、シゾフィランの主鎖3グルコースユニットに1つずつ存在する側鎖グルコース残基への過ヨウ素酸酸化と還元的アミノ化を利用した部位特異的化学修飾法とそれに伴う多糖・核酸複合体の構造安定化に関するものである。過ヨウ素酸酸化は、1,2-ジオールにおけるジオール間の結合を開裂させ、2つのアルデヒド基を生成させる。シゾフィランの主鎖には1,2-ジオールは存在せず、過ヨウ素酸酸化はシゾフィランにおいては側鎖グルコース残基でのみ起こる。また、それに引き続く還元的アミノ化はアルデヒドとアミンのシッフ塩基形成を通じて起こる反応であり、過ヨウ素酸酸化の起こった側鎖でのみこの反応は起こる。本手法では過ヨウ素酸酸化反応を制御することで任意の割合の側鎖にアミノ基を導入することに成功した。
|











