がん遺伝子RASによるがん悪性化機構の
解明と制御法の開発

がん遺伝子RASによるがん悪性化機構の解明と制御法の開発
フロンティアサイエンス学部 生命化学科 准教授
がん遺伝子RAS
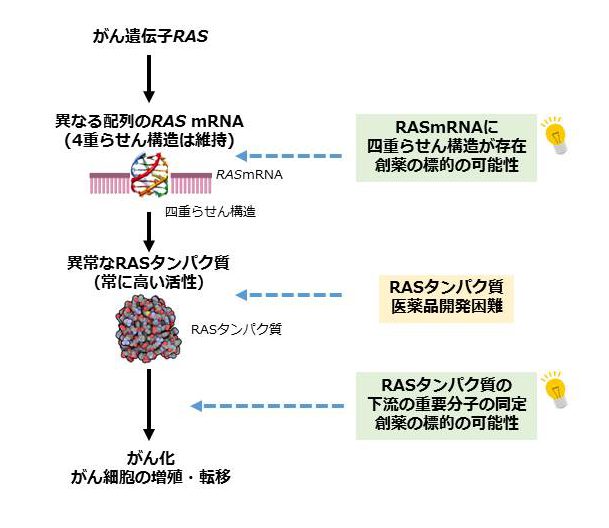
がん細胞は、いくつかの特定の遺伝子に傷がつくことが原因となり正常細胞から変化したものです。この特定の遺伝子の中の代表的なものに、RAS遺伝子があります。傷ついたRAS遺伝子は、がん化やがん細胞の悪性化(高い浸潤能・転移能の獲得)のアクセル役となるがん遺伝子として働きます。これは、がん遺伝子RASから作られるRAS mRNAにも傷が受け継がれ、そのmRNAから作られるRASタンパク質は、活性化した状態が維持される異常なRASタンパク質となるからです。われわれは、異常なRASタンパク質が誘導するがん悪性化のプロセスを壊す方法やRASタンパク質の量を減らす方法を見つけることで、画期的ながんの治療法の開発を目指しています。
がん遺伝子RASがアクセルを踏むメカニズム
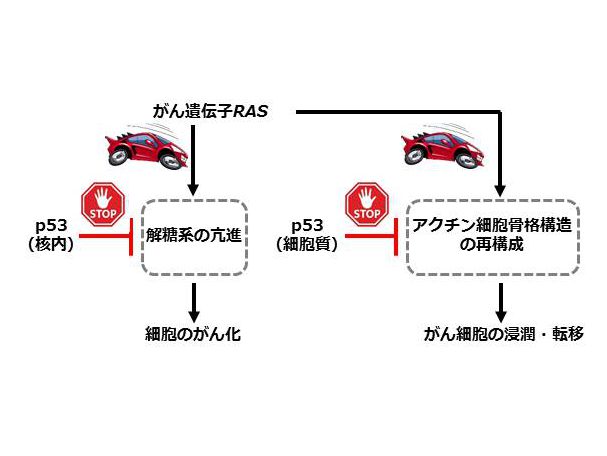
ブレーキ役のがん抑制遺伝子p53が正常に働いている間、がん遺伝子RASはがん化のアクセルを踏むことができません。p53によるブレーキが解除され、がん細胞特有の代謝様式ワーブルグ効果が形成されることが、がん化に必要であることを明らかにしました。この研究成果は、英国科学誌Nature Cell Biologyと米国科学アカデミー紀要(PNAS)に掲載されました。また、がん遺伝子RASは、がん細胞の悪性化を促進します。このRASの働きに対しても、p53は細胞の形や動きをコントロールすることでブレーキをかけていることを明らかにしました。この研究成果は、米国科学誌Journal Cell Biologyなどに掲載されました。
RASmRNAを狙ったがん治療法の開発
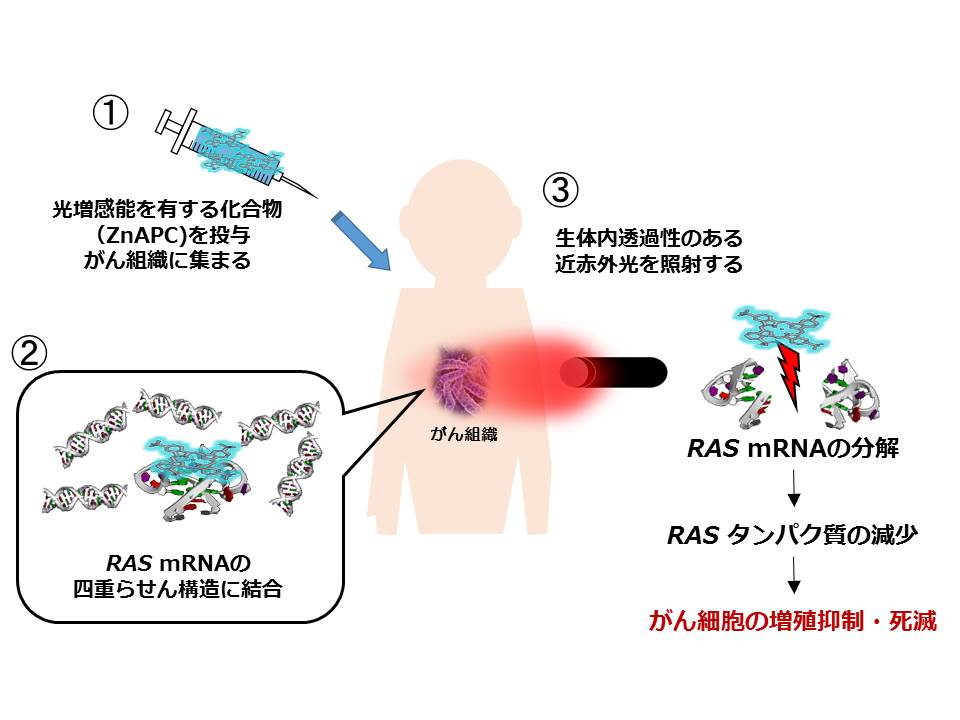
RASタンパク質を狙った治療薬の開発は、世界中で長年行われてきました。しかし、RASタンパク質の構造上の特徴から開発が難しく、実際に治療に使われている薬は未だにありません。そこで、RASタンパク質のもとになるRASmRNAがもっている特別な構造(四重らせん構造)を狙って壊す方法をフロンティアサイエンス学部の三好大輔教授、赤松謙介教授、鶴岡孝章准教授と先端生命工学研究所の杉本直己所長と建石寿枝講師との共同で開発しました。四重らせん構造に結合する光感受性物質をがん細胞にとりこませ、赤い光を照射すると、RASmRNAは切断され、その結果RASタンパク質の量が減少し、細胞は死滅します。この研究成果は、英国科学誌Nature Communicationsに掲載され、50社以上のメディアで取り上げられました。